Proses Pembakaran Batubara
Pembakaran pada bahan bakar batubara merupakan proses pelepasan energi panas yang dihasilkan dari reaksi combustible material dengan oksida (oksigen dalam udara). Tujuan utama dari proses pembakaran adalah memaksimalkan pelepasan energi dengan meminimalkan kerugian-kerugian yang mungkin timbul selama proses pembakaran. Faktor utama yang mempengaruhi proses pembakaran antara lain :
- Temperature, yaitu suhu yang cukup untuk terjadinya penyalaan dan menjaga penyalaan bahan bakar.
- Turbulence, efek turbulensi akan berpengaruh terhadap pencampuran antara serbuk batubara dengan oksigen pada udara. Turbulensi yang baik menghasilkan campuran yang merata sehingga mengurangi kerugian akibat un-burnt carbon.
- Time, adalah kecukupan waktu untuk terjadinya tahapan-tahapan proses pembakaran hingga semua combustible material bereaksi sempurna dengan oksigen dan melepaskan energi panas.
- Oxygen, merupakan reaktan utama pada reaksi pembakaran sehingga kecukupan oksigen sangat berpengaruh terhadap kesempurnaan pembakaran. Oleh karena itu dalam aplikasinya selalu digunakan excess air (oksigen berlebih) untuk menjamin kecukupan oksigen untuk reaksi.
Reaksi utama pada proses pembakaran batubara terdiri dari reaksi combustible material (C, H, dan S) dengan oksigen yang menghasilkan produk pembakaran sempurna berupa gas CO2 dan H2O. Persamaan reaksi pembakaran dapat dituliskan sesuai persamaan 1 sampai 3 sebagai berikut,
2H + O2 –> 2H2O (1)
2H + O2 –> 2H2O (2)
C + O2 –> CO2 (3)
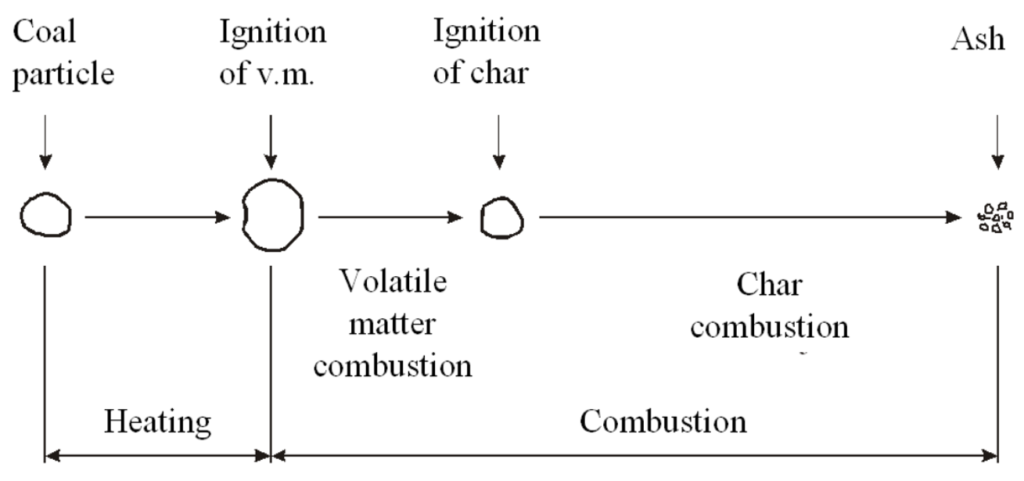 Gambar 1. Proses pembakaran batubara
Gambar 1. Proses pembakaran batubara
1. Drying
Drying merupakan proses awal batubara untuk menghilangkan moisture yang terkandung pada permukaan ataupun pada pori-pori batubara. Proses pengeringan ini terjadi sebelum batubara bercampur dengan udara pembakaran di furnace. Pengeringan dimulai pada saat batubara bercampur dengan primary air di mill, sedangkan sisa moisture yang terletak dalam pori-pori yang sangat kecil pada batubara akan dikeringkan di dalam furnace karena membutuhkan temperatur yang lebih tinggi untuk menguapkan moisture tersebut.
2. Devolatilisasi/Pirolisis
Setelah kadar air dihilangkan maka temperatur dari partikel semakin meningkat sehingga partikel mulai terdekomposisi dan terjadi proses pelepasan zat–zat yang mudah menguap (volatile matter). Volatile matter merupakan bagian dari bahan bakar padat yang bisa terbakar. Bagian ini terdiri dari bagian yang ringan sampai berat. Bagian yang ringan akan menguap terlebih dahulu. Volatile matter keluar rongga bahan bakar dan memenuhi pori-pori. Hal ini menyebabkan oksigen dari luar tidak dapat masuk kedalam partikel. Pada tahap ini terjadi pemanasan partikel tanpa kehadiran oksigen yang disebut pirolisis. Sebagian dari gas hasil pirolisis bereaksi dengan air dan gas produk pirolisis lain. Tabel 1 menunjukkan reaksi- reaksi yang terjadi selama pirolisis.
Tabel 1 Reaksi Kimia pada proses devolatilisasi/pirolisis
| Carbon–oxygen reaction | C + ½ O2 → CO |
| Boudouard reaction | C + CO2 → 2CO |
| Carbon water reaction | C + H2O → CO + H2 |
| Hydrogenation reaction | C + 2H2 → CH4 |
| Water – gas shift reaction | CO + H2O → CO2 + H2 |
| Methanation | CO + 3H2 → CH4 +H2O |
Hasil pirolisis terbakar dan membentuk nyala yang memperbesar devolatilisasi. Pada bagian yang lain uap air akan mengalir keluar melewati pori-pori sehingga temperatur pembakaran turun. Setelah seluruh air keluar maka nyala api akan lebih besar dan temperatur naik.
3. Pembakaran Char (Kabon Tetap)
Char atau fixed carbon merupakan gumpalan matriks karbon dengan sedikit hidrogen yang terdapat pada senyawa bahan bakar. Bagian ini sangat berpori yang berarti luas permukaan bagian dalam sangat besar. Jika terdapat oksigen maka akan terjadi pembakaran pada char. Char memiliki nilai kalor yang paling tinggi dibandingkan dengan volatile matter. Ketika terjadi pembakaran pada char, maka temperatur akan naik lebih tinggi dari sekitarnya. Proses ini merupakan tahapan akhir dari proses pembakaran pada bahan bakar padat.
Temperatur nyala adalah temperatur pada saat jumlah zat mudah terbakar meningkat secara cepat dan tepat sebelum bereaksi dengan oksigen secara kimia. Setiap unsur memiliki temperatur nyala yang berbeda, misalnya karbon (C) memiliki temperatur nyala sekitar 343 oC. Pada kondisi nyata, setiap zat tidak terbakar secara tepat pada temperatur nyala. Bentuk ruang bakar, rasio udara terhadap bahan bakar dan beragam dampak dari campuran zat yang mudah terbakar mempengaruhi temperatur nyala. Temperatur nyala bahan bakar batubara umumnya berada pada temperatur nyala karbon. Komponen volatil pada bahan bakar batubara akan terlepas seiring dengan peningkatan temperatur, namun tidak akan terbakar sebelum temperatur nyala tercapai.